سلول های بنیادی در بیماری های سیستم عصبی مرکزی: استراتژی های درمانی امیدوارکننده
بیماری های سیستم عصبی مرکزی (CNS) عامل اصلی مرگ و میر و ناتوانی هستند.
با توجه به اینکه نورون های CNS در هنگام بلوغ توانایی خود تجدید و بازسازی ندارند، از دست دادن آنها پس از آسیب یا بیماری غیرقابل برگشت است. اغلب منجر به اختلالات عملکردی می شود.
متأسفانه، گزینههای درمانی برای بیماریهای CNS هنوز محدود است و درمانهای مؤثر برای این بیماریهای بدنام باید مورد بررسی قرار گیرند.
درمان با سلول های بنیادی به عنوان یک استراتژی درمانی بالقوه برای بهبود پیش آگهی بیماری های CNS ظاهر شده است.
انباشته شدن شواهد بالینی و بالینی نشان داده است که مکانیسمهای مولکولی متعدد، مانند جایگزینی سلول، تنظیم ایمنی و اثر نوروتروفیک، زمینه ساز استفاده از درمان با سلولهای بنیادی برای بیماریهای CNS است.
این مقاله مروری با هدف خلاصه کردن نقش و مکانیسم های اساسی درمان با سلول های بنیادی در درمان بیماری های CNS است. و ارزش ارزیابی بیشتر برای کاربردهای درمانی بالقوه درمان سلول های بنیادی در بیماری CNS را دارد.
بیماری های سیستم عصبی مرکزی (CNS)
بیماریهای CNS از شایعترین اختلالاتی هستند که بر سیستم عصبی تأثیر میگذارند و منجر به آسیب غیرقابل برگشت و از دست دادن عملکرد میشوند.
این بیماری ها با نرخ بالای مرگ و میر و ناتوانی همراه هستند و بار قابل توجهی را بر جامعه تحمیل می کنند
اعتقاد بر این بود که نورونهای موجود در CNS پستانداران بالغ فاقد توانایی بازسازی خود به خود به دنبال آسیب هستند.
گزینههای درمانی برای بیماریهای CNS اغلب توسط مکانیسمهای پیچیده و ناقص شناختهشده در زمینه پاتوژنز آنها با مانع مواجه میشوند.
صدمات CNS مانند سکته مغزی، آسیب نخاعی (SCI) و آسیب مغزی تروماتیک (TBI) باعث ایجاد یک آبشار از رویدادهای مضر می شود که به شدت بر سلامت عصبی تأثیر می گذارد.
در نتیجه، نیاز مبرمی به استراتژیهای درمانی وجود دارد که بتواند ترمیم عملکرد عصبی در CNS را تسهیل کند.
درمان با سلول های بنیادی
درمان با سلول های بنیادی به عنوان یک روش درمانی آینده نگر برای بیماری های CNS توجه قابل توجهی را به خود جلب کرده است.
سلولهای بنیادی مورد استفاده شامل سلولهای بنیادی جنینی (ESCs)، سلولهای بنیادی پرتوان القایی (iPSCs)، سلولهای بنیادی عصبی (NSCs)، سلولهای بنیادی مزانشیمی (MSCs) و سایر انواع سلولهای بنیادی هستند.
سلول های بنیادی مزانشیمی
سلول های بنیادی مزانشیمی توانایی خود نوسازی و تمایز چند جهت به انواع سلولی را دارند و می توانند تقریباً از هر نوع بافتی مشتق شوند.
علاوه بر این، سلولهای بنیادی مزانشیمی از طریق ترشح فاکتورهای رشد نوروتروفیک و مکانیسمهای دیگر عملکرد محافظتی عصبی را اعمال میکنند.
درمان با سلول های بنیادی برای بیماری های عصبی
درمان با سلول های بنیادی به عنوان یک رویکرد ارزشمند در درمان بیماری های مختلف CNS، به ویژه بیماری های نورودژنراتیو ظاهر شده است.
بیماری های عصبی با انحطاط پیشرونده و از دست دادن نورون ها از نظر ساختار، عملکرد یا کمیت مشخص می شوند.
PD، AD و ALS سه بیماری اصلی تخریب کننده عصبی هستند. درمانهای دارویی و مداخلات جراحی فعلی برای بیماریهای عصبی قادر به متوقف کردن مؤثر فرآیندهای دژنراتیو نیستند.
امروزه، درمان با سلول های بنیادی استراتژی های امیدوارکننده ای را برای رسیدگی به طیف گسترده ای از بیماری های عصبی ارائه می دهد.
بیماری پارکینسون
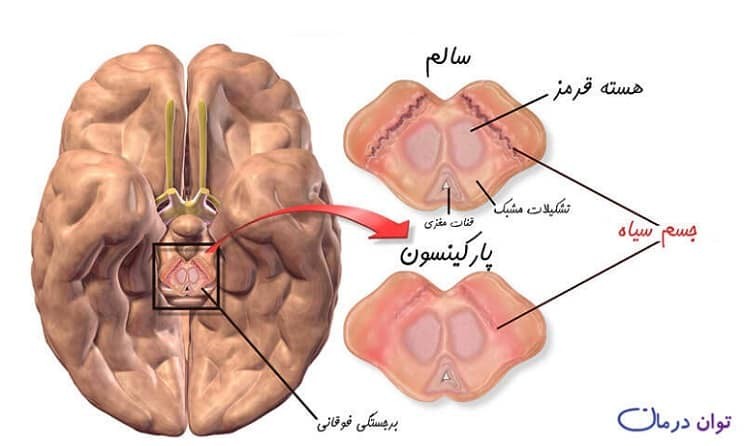
پارکینسون
PD یک اختلال عصبی پیشرونده شایع است که با کمبود دوپامین (DA) در جسم مخطط مشخص میشود.
رویکرد درمانی اولیه فعلی برای PD شامل تجویز لوودوپا، یک پیش ساز DA، برای جبران کمبود DA ناشی از تخریب نورونهای دوپامینرژیک است. در حالی که درمان دارویی می تواند علائم را کاهش دهد، اما پیشرفت تخریب عصبی را متوقف یا معکوس نمی کند.
پیوند نورون های دوپامینرژیک جنینی انسان به جسم مخطط بیماران PD به عنوان یک درمان بالقوه نویدبخش است (Freed et al., 2001). سلولهای بنیادی پیوندی بقای خود را در بیماران مبتلا به PD شدید نشان دادهاند و با موفقیت به نورونهای DA عملکردی تمایز مییابند و تولید DA را ادامه میدهند (Piccini et al., 1999). با این حال، اثربخشی بالینی پیوند سلولهای بنیادی، احتمالاً به دلیل تفاوتهای بین سلولهای پیوندی، متغیر است (Olanow et al., 2003). علیرغم چالشهای موجود در تولید نوع مناسب نورونهای DA و بهبود شرایط برای افزایش بقای سلولهای پیوندی، خوشبینی در مورد پتانسیل سلولهای بنیادی برای القای تولید نورونهای DA کاربردی و خدمت به عنوان نوعی سلول درمانی وجود دارد (کیم، 2011).

بیماری آلزایمر
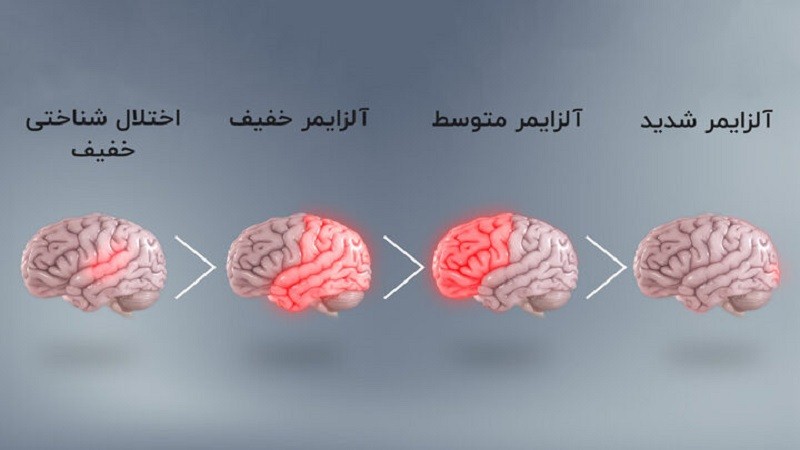
آلزایمر
AD شایع ترین علت زوال عقل است. مکانیسم پاتولوژیک اولیه AD شامل تجمع پروتئین آمیلوئید-β (Aβ) است که منجر به انحطاط و از بین رفتن نورون ها و سیناپس ها در مناطق مختلف مغز می شود.
سیستم کولینرژیک نقش مهمی در تنظیم یادگیری و حافظه دارد. از این رو، استفاده از مهارکنندههای استیل کولین استراز (AChEI) میتواند تا حدی اختلال شناختی را در AD کاهش دهد.
از آنجایی که درمان دارویی برای AD در درجه اول تسکین دهنده است و پیشرفت بیماری را کند یا معکوس نمی کند، گزینه های درمانی موثر برای رفع نیازهای بیماران AD مورد نیاز است.
درمان با سلول های بنیادی برای AD در برآوردن این نیاز نویدبخش است.
پیوند NSCها در افزایش نوروژنز درون زا و جلوگیری از زوال شناختی بیشتر، همانطور که توسط آزمایشات حیوانی مشهود است، نویدبخش بوده است.
با این حال، پتانسیل درمانی NSCs می تواند توسط سطوح پاتولوژیک بالای استرس اکسیداتیو، که می تواند به نورون ها آسیب برساند و اثرات نوروژنیک را مختل کند، متوقف شود.
استراتژیهای کنونی در درجه اول بر هدایت تمایز NSCها به نورونها و بهینهسازی اجزای ریزمحیطی برای تقویت نوروژنز تمرکز دارند.
ادغام پیوند NSC با ویرایش ژن، نانومواد، مداخلات دارویی و سایر رویکردها برای بهبود کارایی درمان با سلول های بنیادی مورد بررسی قرار گرفته است.
با این وجود، انتقال از آزمایشهای حیوانی به کاربردهای بالینی همچنان به تلاشها و تلاشهای تحقیقاتی قابل توجهی نیاز دارد.
رفرنس
Ying C, Zhang J, Zhang H, Gao S, Guo X, Lin J, Wu H, Hong Y. Stem cells in central nervous system diseases: Promising therapeutic strategies. Experimental Neurology. 2023 Sep 22:114543.
لینک مقاله
https://www.sciencedirect.com/science/article/pii/S0014488623002285


